کلید واژه ها:
مدل تعامل فضایی ; مدل سازی فضایی ; COVID-19 ؛ الگوهای مکانی-زمانی
۱٫ مقدمه
۲٫ روش ها
۲٫۱٫ مدل های SIR و SIR-F
مدلهای اپیدمی حساس محفظه قطعی-عفونی-بازیابی شده [ ۳۳ ] مبتنی بر انتقال ویروسی (در این مورد SARS-CoV-2) در یک جمعیت ( N ) از ابتدای قرن بیستم مورد استفاده قرار گرفتهاند و با استفاده از آن توصیف شدهاند. مجموعه ای از معادلات ODE (دیفرانسیل معمولی):
که در آن S ، I و R به ترتیب تعداد افراد مستعد، آلوده و بهبودیافته هستند. N اندازه جمعیت است. نرخ تماس گرفتن «فرکانس تعامل»، نرخ جریان از حساس به آلوده است. نرخ بهبودی، نرخ جریان از آلوده به بهبودیافته یا مرده است. و t نشان دهنده زمان است [ ۳۴ ]. چندین مدل از مدل های پایه SIR مشتق شده است. در این مقاله، ما مدل SIR-F را اعمال میکنیم که جمعیت R (بازیابی شده) را به زیرجمعیتهای بازیابی شده و شکستخورده (درگذشته) تقسیم میکند.
۲٫۲٫ مدل جاذبه
مدل گرانش نامحدود:
مدل محدود تولید (منشا):
مدل محدود مقصد (جاذبه):
مدل دارای محدودیت مضاعف:
فرمول باید بر اساس ضرایب متقابل حاصل از مفهوم گرانش کالیبره شود. برای هر جفت شهرستان i و j ضریب تعامل I ij را به صورت زیر تعیین کردیم:
۲٫۳٫ روش شناسی پذیرفته شده
۳٫ داده ها، آزمایش ها و نتایج
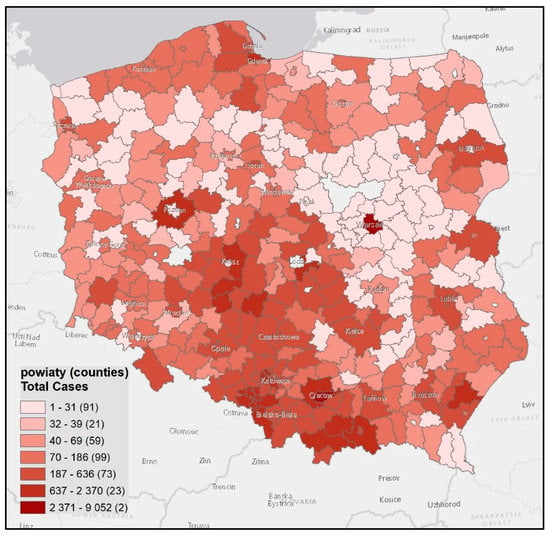
۳٫۱٫ داده ها
۳٫۲٫ کالیبراسیون مدل SIR-F
۳٫۳٫ کالیبراسیون مدل – تعامل فضایی
۳٫۴٫ تایید مدل
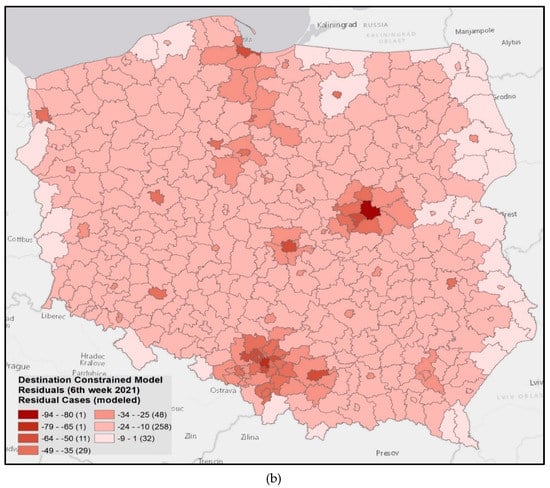
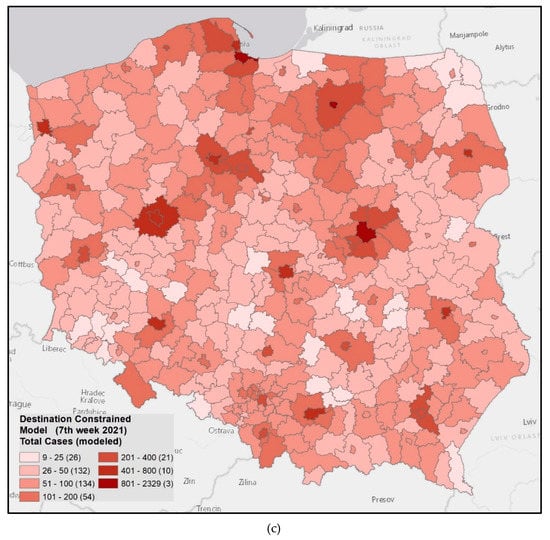
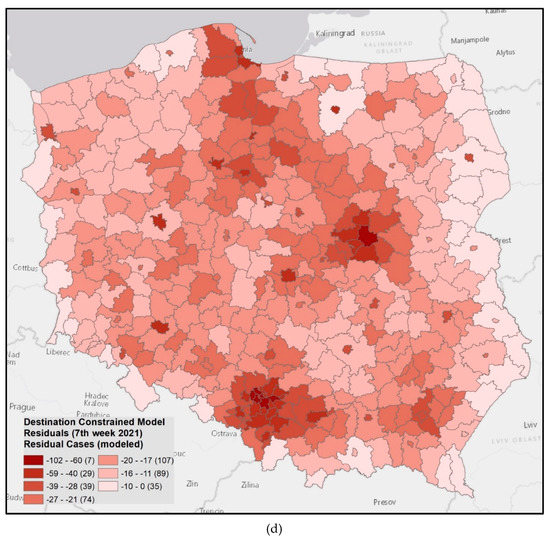
راستیآزمایی مدلهای تعامل فضایی محدود به مقصد برای هفتههای ۶ و ۷ ۲۰۲۱ (۱ تا ۷ فوریه) با استفاده از دادههای تجربی جمعآوریشده عفونتهای COVID-19 بر اساس شهرستان انجام شد. فرمول کلی مدل مقید مقصد (III) برای هفته های ششم و هفتم سال ۲۰۲۱ (معادلات (۹) و (۱۰)):
که در آن T ij تعداد مدلسازیشده عفونتها در تعداد j به دلیل تعامل با شهرستان i است، V i جمعیت شهرستان i است و d ij فاصله بین شهرستان i و j است. برای خود شهرستان، فاصله در نظر گرفته شده شعاع دایره ای با مساحت مساوی تا ناحیه شهرستان بود.
۳٫۵٫ شبیه سازی
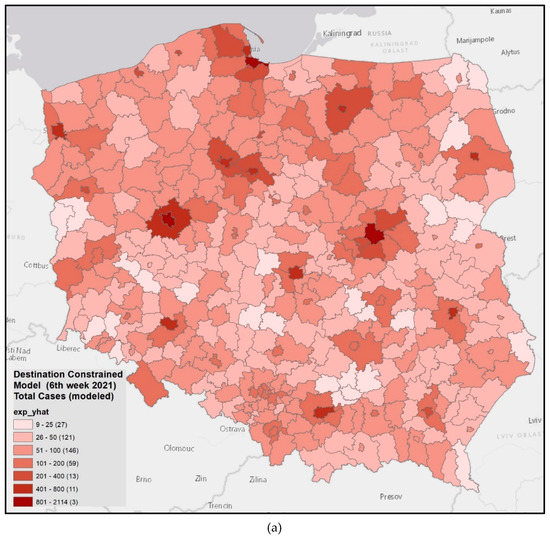
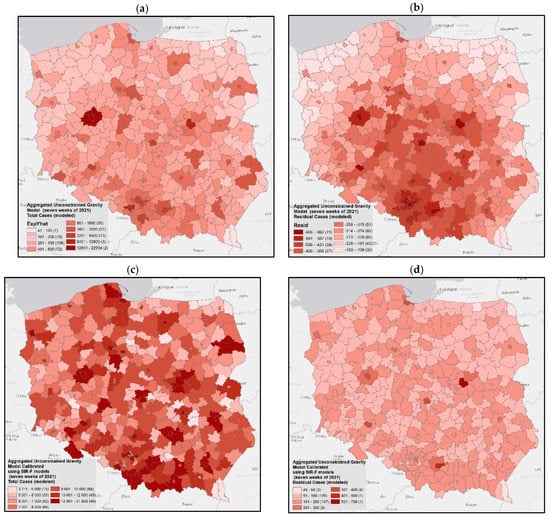
مدلهای گرانش نامحدود برای هفتههای اول (هفتههای ششم و هفتم سال ۲۰۲۱، معادلات (۱۱) و (۱۲) و برای هفت هفته آینده (معادله (۱۳)) شکلهای متفاوتی داشتند. نتایج مدلسازی در نقشهها ارائه شده است ( شکل) ۸ A–D).
که در آن T ij تعداد آلودگی مدل شده است، V i جمعیت شهرستان i است، W j جمعیت شهرستان j ، و d ij فاصله بین شهرستان های i و j است . برای خود شهرستان، فاصله در نظر گرفته شده شعاع دایره ای از مساحت برابر با مساحت شهرستان بود.
۴٫ بحث
۵٫ نتیجه گیری ها
منابع
- Werner, P. ردیابی و مدلسازی عفونتهای همهگیر COVID-19 در لهستان با استفاده از مدلهای تعاملات فضایی. در علوم محاسباتی و کاربردهای آن – ICCSA 2021 ؛ Springer: Cham، سوئیس، ۲۰۲۱٫ [ Google Scholar ]
- رادر، بی. اسکارپینو، اس وی؛ نانده، ا. هیل، آل. ادلام، بی. رینر، RC; پیگوت، دی.م. گوتیرز، بی. زاربسکی، AE; شرستا، م. و همکاران شلوغی و شکل اپیدمی COVID-19. نات. پزشکی ۲۰۲۰ ، ۲۶ ، ۱۸۲۹-۱۸۳۴٫ [ Google Scholar ] [ CrossRef ] [ PubMed ]
- پترسن، ای. کوپمنز، ام. برو، یو. Hamer، DH; پتروسیلو، ن. کاستلی، اف. استورگارد، ام. الخلیلی، س. Simonsen, L. مقایسه SARS-CoV-2 با SARS-CoV و همه گیرهای آنفلوانزا. عفونت لانست دیس ۲۰۲۰ ، ۲۰ ، e238–e244. [ Google Scholar ] [ CrossRef ]
- هوانگ، سی. وانگ، ی. لی، ایکس. رن، ال. ژائو، جی. هو، ی. ژانگ، ال. فن، جی. خو، جی. گو، ایکس. و همکاران ویژگی های بالینی بیماران مبتلا به کروناویروس جدید ۲۰۱۹ در ووهان چین. Lancet ۲۰۲۰ ، ۳۹۵ ، ۴۹۷-۵۰۶٫ [ Google Scholar ] [ CrossRef ][ نسخه سبز ]
- ژو، اف. یو، تی. دو، آر. فن، جی. لیو، ی. لیو، ز. شیانگ، جی. وانگ، ی. آهنگ، بی. گو، ایکس. و همکاران دوره بالینی و عوامل خطر برای مرگ و میر بیماران بزرگسال مبتلا به COVID-19 در ووهان، چین: یک مطالعه کوهورت گذشته نگر. Lancet ۲۰۲۰ ، ۳۹۵ ، ۱۰۵۴-۱۰۶۲٫ [ Google Scholar ] [ CrossRef ]
- چان، JF-W. یوان، اس. کوک، ک.-ح. به، KKW؛ چو، اچ. یانگ، جی. زینگ، اف. BNurs، JL; Yip، CC-Y. پون، RW-S. و همکاران یک خوشه خانوادگی از ذات الریه مرتبط با ویروس کرونای جدید ۲۰۱۹ که نشان دهنده انتقال فرد به فرد است: مطالعه یک خوشه خانوادگی. Lancet ۲۰۲۰ ، ۳۹۵ ، ۵۱۴-۵۲۳٫ [ Google Scholar ] [ CrossRef ][ نسخه سبز ]
- گراسلی، NC; فریزر، سی. مدل های ریاضی انتقال بیماری های عفونی. نات. Rev. Microbiol. ۲۰۰۸ ، ۶ ، ۴۷۷-۴۸۷٫ [ Google Scholar ] [ CrossRef ] [ PubMed ]
- ویلسون، آنتروپی AG در مدلسازی شهری و منطقه ای ; ویلسون، AG، اد. Pion: لندن، بریتانیا، ۱۹۷۰٫ [ Google Scholar ]
- ویلسون، الف. مدلهای اپیدمی با جغرافیا. arXiv ۲۰۲۰ ، arXiv:2005.07673v1. در دسترس آنلاین: https://arxiv.org/abs/2005.07673v1 (در ۴ دسامبر ۲۰۲۱ قابل دسترسی است).
- مارشال، جی.ام. وو، اس ال. سانچز، اس ام. Kiware، SS; اندلوو، م. Ouédraogo، AL; توره، مگابایت؛ استوراک، اچ جی. غنی، AC; فرگوسن، NM مدلهای ریاضی تحرک انسان در ارتباط با انتقال مالاریا در آفریقا. علمی Rep. ۲۰۱۸ , ۸ , ۷۷۱۳٫ [ Google Scholar ] [ CrossRef ] [ PubMed ]
- شیا، ی. بیورنستاد، ON; گرنفل، دینامیک فراجمعیت سرخک BT: یک مدل گرانشی برای جفت و پویایی اپیدمیولوژیک صبح. نات. ۲۰۰۴ ، ۱۶۴ ، ۲۶۷-۲۸۱٫ [ Google Scholar ] [ CrossRef ]
- یان، X.-Y.; ژو، تی. بازی انتخاب مقصد: نظریه تعامل فضایی بر تحرک انسان. علمی جمهوری ۲۰۱۹ ، ۹ ، ۹۴۶۶٫ [ Google Scholar ] [ CrossRef ]
- استوارت، JQ قوانین تجربی ریاضی در مورد توزیع و تعادل جمعیت. Geogr. Rev. ۱۹۴۷ , ۳۷ , ۴۶۱-۴۸۵٫ [ Google Scholar ] [ CrossRef ]
- گریگوری، دی. جانستون، آر. پرت، جی. واتس، ام. علاوه بر این، S. (Eds.) The Dictionary of Human Geography , ۵th ed.; Wiley-Blackwell: Hoboken، NJ، USA، ۲۰۰۹٫ [ Google Scholar ]
- Werner, P. شبیه سازی دسترسی به زیرساخت ICT در لهستان با استفاده از مدل های پتانسیل جغرافیایی. در مجموعه مقالات شانزدهمین کنفرانس بین المللی علم سیستم، Banff، AB، کانادا، ۸-۱۲ مه ۲۰۰۷٫ صص ۲۶۱-۲۶۹٫ [ Google Scholar ]
- Tobler، WR Cellular Geography. در فلسفه در جغرافیا ; Gale, S., Olsson, G., Eds. Springer: Dordrecht، هلند، ۱۹۷۹; صص ۳۷۹-۳۸۶٫ [ Google Scholar ]
- رایلی، اس. ایمز، ک. ایشم، وی. مولیسون، دی. Trapman, P. پنج چالش برای مدلهای اپیدمی فضایی. اپیدمی ۲۰۱۵ ، ۱۰ ، ۶۸-۷۱٫ [ Google Scholar ] [ CrossRef ] [ PubMed ][ نسخه سبز ]
- Rossa، FD; سالزانو، دی. دیمگلیو، ا. برناردو، MD; دی للیس، ام. کوراجو، ام. کالابرس، سی. گوارینو، آ. کاردونا-ریورا، آر. دی للیس، پی. و همکاران یک مدل شبکه ای از ایتالیا نشان می دهد که استراتژی های منطقه ای متناوب می تواند اپیدمی COVID-19 را کاهش دهد. نات. اشتراک. ۲۰۲۰ ، ۱۱ ، ۵۱۰۶٫ [ Google Scholar ] [ CrossRef ]
- پرینو، اف. زینو، ال. پورفیری، م. Rizzo، A. مدلسازی و پیشبینی تأثیر فاصلهگذاری اجتماعی و محدودیتهای سفر بر شیوع COVID-19. رابط JRS ۲۰۲۱ ، ۱۸ ، ۱۷۵٫ [ Google Scholar ]
- گوسگنز، ام. هندریکس، تی. بون، ام. استین باکرز، دبلیو. هیستربیک، اچ. ون در هافستاد، آر. Litvak، N. معاوضه بین محدودیت های تحرک و انتقال SARS-CoV-2. رابط JRS ۲۰۲۱ ، ۱۸ ، ۱۷۵٫ [ Google Scholar ] [ CrossRef ]
- جووردانو، جی. بلانچینی، اف. برونو، آر. کولانری، پ. دی فیلیپو، آ. دی متئو، آ. کولانری، ام. مدلسازی اپیدمی COVID-19 و اجرای مداخلات گسترده جمعیت در ایتالیا. نات. پزشکی ۲۰۲۰ ، ۲۶ ، ۸۵۵-۸۶۰٫ [ Google Scholar ] [ CrossRef ] [ PubMed ]
- دنجرموند، جی. دی ویتو، سی. Pesaresi, C. استفاده از GIS در زمان بحران COVID-19، نگاهی به آینده. یک بحث مشترک J-READING J. Res. دیدات. Geogr. ۲۰۲۰ ، ۱ ، ۱۹۵-۲۰۵٫ [ Google Scholar ]
- Boulos، MN; Geraghty، EM ردیابی و نقشه برداری جغرافیایی بیماری کرونا ویروس کووید-۱۹/سندرم حاد تنفسی ویروس همه گیر ۲ (SARS-CoV-2) و رویدادهای مرتبط در سراسر جهان: چگونه فن آوری های GIS قرن بیست و یکم از مبارزه جهانی علیه شیوع و همه گیری ها حمایت می کنند. بین المللی J. Health Geogr. ۲۰۲۰ ، ۱۹ ، ۸٫ [ Google Scholar ]
- اسارسی، ج. پاویا، دی. دی ویتو، سی. باربارا، ا. سرابونا، وی. دی روزا، ای. شبیه ساز انتشار فضا-زمان پویا در یک محیط GIS برای مقابله با اضطراری Covid-19. آزمایش یک برنامه ژئوتکنولوژی در رم. Geogr. فنی ۲۰۲۱ ، ۱۶ ، ۸۲-۹۹٫ [ Google Scholar ]
- فرانک-پاردو، آی. ناپلتانو، بی.ام. روزت ورجز، اف. Billa, L. تجزیه و تحلیل فضایی و GIS در مطالعه COVID-19. بازنگری. علمی کل محیط. ۲۰۲۰ , ۷۳۹ , ۱۴۰۰۳۳٫ [ Google Scholar ] [ CrossRef ] [ PubMed ]
- هول، ا. دلمل، EM; Desjardins، MR; Lan, Y. نظارت روزانه COVID-19 با استفاده از آمار اسکن فضا-زمان آینده نگر در ایالات متحده. تف کردن اپیدمیول فضایی-زمانی. ۲۰۲۰ ، ۳۴ ، ۱۰۰۳۵۴٫ [ Google Scholar ] [ CrossRef ] [ PubMed ]
- احسن، ر. حسین، MM استفاده از GIS و تجزیه و تحلیل فضایی برای تصمیم گیری آگاهانه در همه گیری COVID-19. فناوری سیاست سلامت ۲۰۲۱ ، ۱۰ ، ۷٫ [ Google Scholar ] [ CrossRef ] [ PubMed ]
- وو، زی. McGoogan، JM ویژگی ها و درس های مهم شیوع بیماری کروناویروس ۲۰۱۹ (COVID-19) در چین: خلاصه گزارش ۷۲۳۱۴ مورد از مرکز چین برای کنترل و پیشگیری از بیماری. جاما ۲۰۲۰ ، ۳۲۳ ، ۱۲۳۹–۱۲۴۲٫ [ Google Scholar ] [ CrossRef ] [ PubMed ]
- ژانگ، ایکس. رائو، اچ. وو، ی. هوانگ، ی. دای، اچ. مقایسه ویژگیهای مکانی و زمانی شیوع کووید-۱۹ و سارس در سرزمین اصلی چین. BMC Infect Dis. ۲۰۲۰ ، ۲۰ ، ۸۰۵٫ [ Google Scholar ] [ CrossRef ] [ PubMed ]
- برائر، اف. کاستیلو چاوز، سی. مدل های ریاضی در زیست شناسی جمعیت و اپیدمیولوژی ؛ متون در ریاضیات کاربردی; Springer: New York, NY, USA, 2012; جلد ۴۰ شابک ۹۷۸-۱-۴۶۱۴-۱۶۸۵-۲٫ [ Google Scholar ]
- دوان، دبلیو. فن، ز. ژانگ، پی. گوا، جی. کیو، X. رویکردهای ریاضی و محاسباتی به مدلسازی اپیدمی: مروری جامع. جلو. محاسبه کنید. علمی ۲۰۱۵ ، ۹ ، ۸۰۶-۸۲۶٫ [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Casetti، E. روش گسترش، وابستگی، و چند مدل سازی. در کتابچه راهنمای تحلیل کاربردی فضایی ; Fischer, MM, Getis, A., Eds. Springer: برلین/هایدلبرگ، آلمان، ۲۰۱۰; صص ۴۸۷-۵۰۵٫ شابک ۹۷۸-۳-۶۴۲-۰۳۶۴۶-۰٫ [ Google Scholar ]
- کرماک، WO; McKendric، AG سهمی در نظریه ریاضی اپیدمی ها. Proc. R. Soc. لندن. سر. حاوی. پاپ یک ریاضی فیزیک شخصیت ۱۹۲۷ ، ۱۱۵ ، ۷۰۰-۷۲۱٫ [ Google Scholar ] [ CrossRef ][ نسخه سبز ]
- عبادی، ع. برتولوتی، پی. دینر، بی. شاه، دی. مدلسازی و تخمین اپیدمی. ۲۰۲۰٫ در دسترس آنلاین: https://idss.mit.edu/wp-content/uploads/2020/04/04.28.2020Epidemic_Modeling_A_Memo.pdf (دسترسی در ۴ دسامبر ۲۰۲۱).
- اوشان، TM یک آغازگر برای کار با ماژول مدلسازی تعامل فضایی (SpInt) در کتابخانه تحلیل فضایی پایتون (PySAL). منطقه ۲۰۱۶ ، ۳ ، R11–R23. [ Google Scholar ] [ CrossRef ]
- مک فادن، دی. تحلیل لوجیت شرطی رفتار انتخاب کیفی. در مرزها در اقتصاد سنجی ; Zarembka، P.، Ed. مطبوعات آکادمیک: نیویورک، نیویورک، ایالات متحده آمریکا، ۱۹۷۴; صص ۱۰۵-۱۴۲٫ [ Google Scholar ]
- Akaike, H. نگاهی جدید به شناسایی مدل آماری. IEEE Trans. خودکار کنترل ۱۹۷۴ ، ۱۹ ، ۷۱۶-۷۲۳٫ [ Google Scholar ] [ CrossRef ]
- ری، اس جی. Anselin, L. PySAL: کتابخانه پایتون از روش های تحلیلی فضایی. Rev. Reg. گل میخ. ۲۰۰۷ ، ۳۷ ، ۵-۲۷٫ [ Google Scholar ] [ CrossRef ]
- گزارش Zakażeń Koronawirusem (SARS-CoV-2). ۲۰۲۱٫ در دسترس آنلاین: https://www.gov.pl/web/koronawirus/wykaz-zarazen-koronawirusem-sars-cov-2 (در ۶ دسامبر ۲۰۲۱ قابل دسترسی است).
- موریل، آر. گیل، جی. Thrall، G. انتشار فضایی. در وب کتاب علوم منطقه ای ; دانشگاه ویرجینیای غربی: مورگانتاون، WV، ایالات متحده آمریکا، ۲۰۲۰٫ [ Google Scholar ]
- ویلسون، سیستمهای فضایی پیچیده AG : مبانی مدلسازی تحلیل شهری و منطقهای . آموزش پیرسون: لندن، بریتانیا، ۲۰۰۰٫ [ Google Scholar ]
- O’Kelly، ME مدل های تعامل فضایی. در دایره المعارف بین المللی جغرافیای انسانی ; کیچین، آر.، ترایفت، ن.، ویرایش. الزویر: آمستردام، هلند، ۲۰۰۹; صص ۳۶۵-۳۶۸٫ [ Google Scholar ]
- ویروس کرونا: اطلاعات و توصیهها محدودیت های موقت ۲۰۲۱٫ در دسترس آنلاین: https://www.gov.pl/web/coronavirus/temporary-limitations (در ۶ دسامبر ۲۰۲۱ قابل دسترسی است).
- داده های دولتی در توییتر به اشتراک گذاشته شده است. در دسترس آنلاین: https://twitter.com/MZ_GOV_PL (در ۸ دسامبر ۲۰۲۱ قابل دسترسی است).
- Główny Urząd Geodezji i Kartografii. ۲۰۲۱٫ در دسترس آنلاین: http://www.gugik.gov.pl/pzgik/inne-dane-udostepniane-bezplatnie (در ۴ دسامبر ۲۰۲۱ قابل دسترسی است).
- بانک دانیچ لوکالنیچ GUS. ۲۰۲۱٫ در دسترس آنلاین: https://bdl.stat.gov.pl/BDL/start (در ۴ دسامبر ۲۰۲۱ قابل دسترسی است).
- تیم توسعه CovsirPhy. CovsirPhy، بسته پایتون برای تجزیه و تحلیل COVID-19 با مدلهای ODE مشتق شده از SIR. ۲۰۲۰٫ در دسترس آنلاین: https://github.com/lisphilar/covid19-sir (در ۴ دسامبر ۲۰۲۱ قابل دسترسی است).
- گیدوتی، ای. Ardia, D. Covid-19 Data Hub. J. نرم افزار منبع باز. ۲۰۲۰ ، ۵ ، ۲۳۷۶٫ [ Google Scholar ] [ CrossRef ]
- Fotheringham، AS; مدلهای تعامل فضایی O’Kelly، ME : فرمولبندیها و کاربردها . ناشران آکادمیک Kluwer: Alphen aan Den Rijn، هلند، ۱۹۸۹٫ [ Google Scholar ]
- شرح مدل ICM UW-COVID. در دسترس آنلاین: https://covid-19.icm.edu.pl/ (در ۴ دسامبر ۲۰۲۱ قابل دسترسی است).
- زو، دی. بله، X. Manson, S. افشای الگوی تغییر فضایی همهگیری COVID-19 در ایالات متحده. علمی Rep. ۲۰۲۱ , ۱۱ , ۸۳۹۶٫ [ Google Scholar ] [ CrossRef ] [ PubMed ]
- مانگو، م. دزوبو، م. چیتونگو، آی. Dzinamarira، T. عوامل خطر COVID-19 در بین کارکنان بهداشت: یک بررسی سریع. Saf. Health Work ۲۰۲۰ , ۱۱ , ۲۶۲-۲۶۵٫ [ Google Scholar ] [ CrossRef ] [ PubMed ]
- طهماسبی، پ. شکری کوهنی، س.م. سهیمی، م. شکری، ن. عوامل محیطی، اقتصادی و بهداشتی چگونه بر آسیبپذیری منطقهای در برابر COVID-19 تأثیر میگذارند؟ MedRxiv ۲۰۲۰ . موجود به صورت آنلاین: https://www.medrxiv.org/content/10.1101/2020.04.09.20059659v1 (در ۲۳ نوامبر ۲۰۲۱ قابل دسترسی است).
- ورنر، پی. اسکرینیک، او. پورچک، ام. Szczepankowska-Bednarek، U. اولشفسکی، آر. Kęsik-Brodacka، M. اثرات آب و هوا و زیست اقلیم بر موارد COVID-19 در لهستان. Remote Sens. ۲۰۲۱ , ۱۳ , ۴۹۴۶٫ [ Google Scholar ] [ CrossRef ]







بدون دیدگاه